大腸ポリープ6 大腸悪性リンパ腫
悪性リンパ腫は、リンパ球が悪性化した腫瘍です。主にリンパ節などリンパ組織内で増殖しますが、消化管の粘膜、粘膜下層のリンパ装置原発のものも少なくありません。さまざまな形態をとり、潰瘍となったりポリープとなったりします(このサイトでは、便宜上「大腸ポリープの章」としました。)。
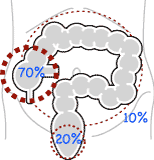
いちばん多いのは胃で、消化管原発悪性リンパ腫の60%をしめます。大腸ではリンパ装置が発達している盲腸(回盲部ふくむ)が7割、直腸肛門部が2割です(図1![]() )。
)。
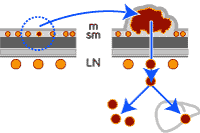
大腸に発生した悪性リンパ腫は大きくなると、腸の外側の所属リンパ節に転移し、さらに遠隔のリンパへと拡がっていきます(図2![]() )。病期がすすむと肝臓や肺、脳など、多臓器への転移がおこります。
)。病期がすすむと肝臓や肺、脳など、多臓器への転移がおこります。
リンパ節原発とくらべると、腸管原発悪性リンパ腫は化学療法がよくききます。ここでは大腸原発の悪性リンパ腫について解説します。
症状
初期にはほとんど症状はなく、便潜血検査などで大腸内視鏡検査を受けて偶然発見されることもあります。
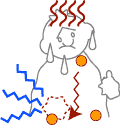
病気が進行すると、体が疲れやすく熱がでます。腹部にしこりを触れたり、鼠径部など体の表面のリンパ節が硬く触れたりします。さらに病気がすすむと、下血したり腸が狭くなることで腹痛や腸閉塞を訴えます(図3![]() )。
)。
診断
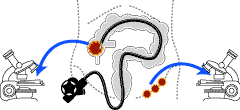
悪性リンパ腫が疑われるときは、まず腫れているリンパ節を摘出して、特殊な染色法で顕微鏡検査にまわします(図4![]() )。同じ悪性リンパ腫といえども悪性度がずいぶんと違いますので、その結果で診断の方針を決定します。
)。同じ悪性リンパ腫といえども悪性度がずいぶんと違いますので、その結果で診断の方針を決定します。
大腸では多くは粘膜より下の層から発生しますので、粘膜下腫瘍の形態をとります。そのため、潰瘍をともなわない例では大腸内視鏡検査で組織を採取しても、一回だけでは明らかな診断がつかないことがあります(図5![]() )。
)。
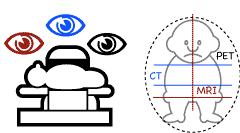
病気の進行度に応じて、治療の方針が大きく変わることがあり、治療前病期診断がたいへん重要です。CT,超音波検査、MRIはリンパ節腫大の有無を見るのに重要です。さらにPETは悪性リンパ腫での検出能が高く特に有用です(図6![]() )。
)。
分類
形態分類
- 限局型
- びまん型
限局型が9割で、腫瘤型、潰瘍型などいろいろな形態をとります。食道や胃の悪性リンパ腫のような「耳たぶに似た形」をとるものはまれです。
組織分類
- ホジキン病
- 非ホジキン病
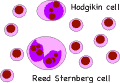
ホジキン細胞や多核細胞(RS細胞)をもつかどうか、で分類します(図7![]() )。特徴的なホジキン細胞をもつものをホジキン病とよびますが、本邦での腸管原発悪性リンパ腫の90%は、非ホジキンB型です。ただし若く発症するときはバーキット型の高悪性度のものがあります。
)。特徴的なホジキン細胞をもつものをホジキン病とよびますが、本邦での腸管原発悪性リンパ腫の90%は、非ホジキンB型です。ただし若く発症するときはバーキット型の高悪性度のものがあります。
治療
基本は抗癌剤をいくつか組み合わせて用いる化学療法です(図8![]() )。ビンクリスチン、エンドキサン、アドリアマイシンにステロイドの4者併用療法はCHOP療法とよばれ、標準治療となっています。
)。ビンクリスチン、エンドキサン、アドリアマイシンにステロイドの4者併用療法はCHOP療法とよばれ、標準治療となっています。
B型リンパ球の表面抗原に対する分子標的薬(rituximab リツキサン)も使われています。B型悪性リンパ腫には効果があり、最近では化学療法と組み合わせて使われることも増えてきました(R-CHOP)。
悪性リンパ腫は放射線の感受性も高いのも特徴です。部位では直腸への放射線療法も効果が十分に期待できます。(図9![]() )
)
胃の悪性リンパ腫も、むかしはまず外科手術で主病巣を切除してから、補助として化学療法をおこなっていました。しかし、最近は化学療法をふくめた集学的治療の成績が向上したため、手術は減っています。